
医療機器の設計と製造はこの10年間で劇的に変化しました。テストコンセプトやプロトタイプのシミュレーションを可能にする3Dプリントおよびソフトウェアアプリケーションの出現により、この分野の組織はより安全な製品をこれまで以上に迅速に市場に投入することができます。汎用性と柔軟性も可能です。ロボットハンドなど、個々の患者に完全に適合する装置を設計し適合させることは、物理的および経済的に実現可能です。エンジニアリングソフトウェアベンダーの多くは、作業を容易にするために非常に貴重なソフトウェアを提供しています。DassaultSystèmesの子会社であるSolidworksは、コンセプトから規制当局の承認に至る医療製品のバリューチェーンを可能にしサポートする、ポートフォリオとして入手可能な一連の製品を開発および製造しています。
エンドツーエンドのツールキット
3Dデザインの作成、シミュレーションの実行、部品表の作成に必要なソフトウェアアプリケーションの一部またはほとんどを提供しているベンダーは数多くありますが、SolidWorksは、ポイントソリューションやPLM(製品ライフサイクル管理)ソフトウェアとは対照的に完全なソリューションを提供する唯一の企業です。Solidworks製品ポートフォリオはPDM(製品開発管理)ソリューションであり、その内容が医療機器開発における2つの重要な成功要因を満たすと確信しています。その要因とはつまり規制要件と市場投入までの時間を指します。
親会社のDassault Systemesは、3Dシステムの世界的リーダーとして認められているため、「3D Experience Company」と呼ばれるほどで「3DS」と略されています。ポートフォリオはCADからビジュアライゼーションおよび3Dプリントの準備まで、あらゆる3Dエンジニアリング支援を提供しますが、その真の強みはそれが生成するドキュメントにあります。旅のすべてのステップは記録され、追跡可能です。これは、規制当局の承認が与えられる場合に不可欠です。
結果に影響を与える要因:規制
医療機器はほとんどの製品よりはるかに厳密なテストと承認を必要としますが、結局のところ、低品質の靴は不快で水疱を生じさせる可能性があり、準標準のステントは患者を殺す可能性すらあります。新しい医療機器を市場に出すための平均的な総コストは、新薬に必要な10億ドルをはるかに下回りますが、規制をクリアするためのコストは、特に医療機関を対象とする場合には、 FDAとデバイスはクラスIIIの機器では総コストの77%にもなることがあります。FDAのクラスIIIの機器は高リスクと見なされ、股関節置換術やステントなど、患者の体内に挿入する必要があり、特別で費用のかかるPMA(市販前承認)が必要な機器です。2010年にPrice Waterhouse Coopersによって発表された報告において議論されているMedical Product Outsourcing Magazineの記事。
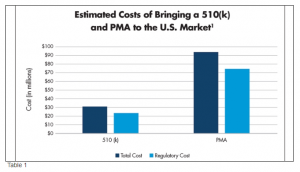
(ソース:https://www.mpo-mag.com/issues/2017-09-01/view_columns/medtech-price-strategies-who-is-going-to-pay-for-it)
報告書は、米国とヨーロッパで新しい医療機器の規制の影響を調べました。米国の患者は、ヨーロッパで機器が承認されてからその機器の使用のメリットを得ることができるようになるまでに、通常さらに2年待たなければならないことが判明しました。
PMAまたは501(k)を取得する際の課題の1つは、関連するすべての文書をまとめてFDAに提出することです。設計から最終プロトタイプまで、ワークフローのすべての詳細が自動的に記録されるため、ここがSolidworksに明らかな利点があります。この機能がなければ、R&Dスタッフは異種システムからのすべてのデータを編集することが必要となります。人手によるオーバーヘッドはプロジェクトに時間を追加し、エラーが発生しやすくなります。必要な文書をすべてまとめて統合することで、ラボでもFDAとの交渉でも時間を節約でき、コストも削減できます。これらの費用の多くは給与に関連しています。従業員の約3分の1が品質管理と規制の順守を担当しています。優れた文書化により、必要な人員が削減されるだけでなく、コンプライアンスの遵守に費やされる時間も削減されるはずです。
結果に影響を与える要因:競争
規制とコンプライアンスによって克服されるべきハードルにもかかわらず、医療製品の世界では競争は厳しいものです。そのため、完成度の高い妥協のない品質とバランスの取れたスピードが不可欠です。コンセプトから3Dレンダリング、FEAやCFDなどのシミュレーションを使用したモデルの反復テスト、包括的な標準部品ライブラリまで、アプリケーションのひとつの統合されたストリームによって、承認および市場投入までの時間が最適化されます。毎回製品全体を扱うのではなく、製品をより小さな部品に分解し、それらを個別にテストしてから一緒にテストすることで、テスト対象を簡素化することでテストを迅速化することもできます。個々の患者に合わせて製品をカスタマイズする機能もDriveworksアプリケーションでは単純化されています。
さまざまな製品を使用している競合他社は、Solidworksのツールが提供するスピードに合わせるのは困難だと考えます。
いくつかのサクセスストーリー
一部の医療機器は製造にステンレス鋼を必要としますが、可能な限りプラスチックが使用されます。プラスチック設計は特殊化されており、例えば射出成形や3Dプリントが必要な場合に、プラスチック部品を製造可能な状態に設計するための特別なツールセットが必要です。DassaultとSolidworksは3Dモデリングのエキスパートであるため、3Dプリンターで印刷できる機器を製造している企業にとっては、これらが最初の選択肢です。
- 3Dプリントが命の恩人である場所の一例として、先天性欠損症の新生児に挿入することができる装置の製造です。一人の幼児は崩れ続ける非常に柔らかい気管を持っていました:副木は風管を保護して強化するために設計され、挿入されました。
- Tensys Medical Incは、非侵襲的動脈血圧管理システムを設計した時に、Solidworksのツールを使用して設計プロセスを60%短縮したと考えています。これにより、競合他社よりも自社製品を突出させることができました。
- 半側麻痺、対麻痺および四肢麻痺の独立した運動を補助するための外骨格は、バイオメカニクスの主要な主題になりつつあります。Solidworks World 2018で、韓国のKyoungchul Kong教授は、同僚の作業者を支援するために設計された2つの外骨格を発表しました。
人間工学に基づいた薬瓶から人工動脈まで、何百もの設計例があり、それらはすべてSolidworksのツールを使用して設計されています。ソフトウェアのコストは、規制をクリアするコストの削減、製品化までの時間の短縮、シミュレーションによるプロトタイプ作成の削減、あるいはそれ3つすべてにおいて簡単に回収できます。すべての製品のライセンスは、サブスクリプション、または永久ライセンス契約のどちらでもかまいません。一部のアプリケーションでは、短期プロジェクト用に製品を必要とする中小企業向けに特別に調整された3か月のサブスクリプションのオプションもあります。ライセンス管理はFlexeraによって提供されていますが、OpenLMはすべてのSolidworks製品すべてのライセンスを管理できます。

